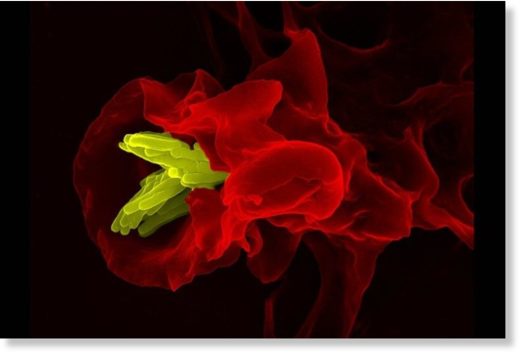
© ZEISS Microscopy / Flickr.comМакрофаг, поглощающий бактерии
Уборкой мёртвых клеток, обломков мембран и прочего мусора у нас занимаются специальные иммунные клетки макрофаги - всё ненужное они в прямом смысле поедают, то есть захватывают клеточными выростами, погружают внутрь себя и переваривают. (Кстати, поедают они не только остатки мёртвых клеток, но и вполне живых бактерий, раковые клетки и вообще всё, что вызывает подозрение.) Макрофаги активно перемещаются в поисках чего бы съесть, и в нашем теле нет такого места, где бы их не было. Есть они и в мозге, только здесь клетки типа макрофагов называются микроглией, причём в мозге они не только следят за чистотой, но и редактируют нейронные цепочки.
При болезни макрофагов становится больше - они приходят к очагу воспаления из костного мозга. И в мозге происходит то же самое: при болезни Альцгеймера, при инсульте, при рассеянном склерозе клеток-уборщиков в нём становится больше. Но, быть может, то увеличение числа макрофагов в очаге болезни - это лишь результат перегруппировки клеток внутри мозга? И, может быть, макрофаги извне в мозг вообще не проникают, и он в любой ситуации старается обходиться только собственной микроглией? В конце концов, многие слышали, что в кровеносных сосудах мозга есть так называемый гематоэнцефалический барьер с очень, очень избирательной проницаемостью, который не даёт проникнуть в мозг многим молекулам и клеткам, плавающим в крови.
Исследователи из Боннского университета, Университета Иены и их коллеги из других научных центров Германии и США нашли способ пометить у мышей стволовые клетки красного костного мозга, которые производили макрофаги. Клетки снабжали геном, который кодировал флуоресцентный белок и который активировался под действием определённого вещества. Включая ген флуоресцентного белка в тот или иной период жизни мыши, можно было увидеть, как распространяются по телу макрофаги, рождённые костном мозге.
Если бы в мозге были иммунные клетки, пришедшие извне, это можно было бы увидеть по их свечению. Но, как говорится в статье в
Nature Neuroscience, у обычных, здоровых мышей мозг не светился - то есть ему хватало тех макрофагов, что у него была. Как уже было сказано, такие постоянно живущие (или резидентные) макрофаги есть во всех тканях (только в мозге они называются микроглией), и ещё раньше тем же исследователям удалось показать, что первые из этих иммунных клеток приходят на свою территорию ещё во время эмбрионального развития и дальше обходятся своими силами. Макрофаги умеют сами делиться, и более новые клетки постепенно замещают старые, не нуждаясь в подкреплении из костного мозга - и в мозге происходит то же самое, что и в прочих органах.
Но в случае чего-то чрезвычайного подкрепление всё-таки появляется. Когда мышам в опыте устраивали инсульт, то больной мозг начинал светиться новыми макрофагами, которые пришли из костного мозга. Поначалу их можно было найти как в живой, так и в мёртвой нервной ткани, но спустя несколько дней все иммунные клетки-«пришельцы» группировались только в мёртвых зонах, где нужно было убрать погибшие нервные клетки.
Также удалось показать важность одного из генов, который помогает иммунным клеткам идти туда, куда нужно, и убирать то, что нужно. Это ген Cxcr4, который кодирует один из поверхностных рецепторов. Если у макрофагов его выключали, то, во-первых, их после инсульта приходило в мозг меньше обычного, а во-вторых, макрофаги никак не могли сгруппироваться в нужном месте - многие из них оставались в здоровых участках мозга, где их помощь была не нужна. Наконец, у макрофагов с выключенным рецептором Cxcr4 оставались малоактивными гены, которые помогают больной ткани справиться с повреждениями, и одновременно у них слишком активировались гены, стимулирующие воспаление - что не очень хорошо, поскольку воспаление бьёт по здоровым клеткам.
Если говорить о практических выводах, то можно сказать, что для эффективного восстановления после инсульта нужно следить за тем, как работает иммунитет: с одной стороны, в мозге должны появиться клетки-помощники, которые уберут молекулярно-клеточный мусор, с другой стороны, эти помощники должны работать только там, где нужно, держа воспалительную реакцию под контролем. Возможно, с помощью каких-нибудь веществ, позволяющих управлять макрофагами, можно будет в перспективе значительно ускорять послеинсультное восстановление мозга.
Комментарии читателей
на нашу рассылку